- 首頁(yè)
- 科研產(chǎn)品
ELISA試劑盒
PCR試劑盒
生化試劑盒
細(xì)胞系
細(xì)胞庫(kù)
基礎(chǔ)培養(yǎng)基
完全培養(yǎng)基
原代細(xì)胞
細(xì)胞專用培養(yǎng)基
菌株
生化試劑
病理染色液
科研抗體
標(biāo)準(zhǔn)品
血清
- 公司簡(jiǎn)介
- 公司新聞
- 技術(shù)服務(wù)
- 代理品牌
- 訂購(gòu)中心
- 加入通蔚
發(fā)布時(shí)間:2024-03-19 發(fā)布作者:通蔚生物
使用免疫化學(xué)的抗體技術(shù)已成為生命科學(xué)研究許多領(lǐng)域的重要工具。免疫化學(xué)的基本原理是“特異性抗體與特異性抗原結(jié)合,形成獨(dú)特的抗原抗體復(fù)合物組合。” 在這篇文章中,我們將解釋抗原抗體復(fù)合物形成過(guò)程中涉及的“抗原抗體相互作用”。
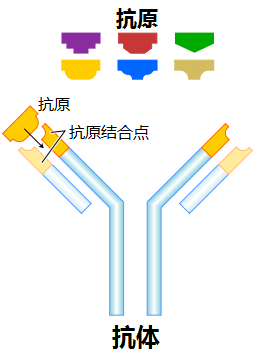
抗原上的抗原位點(diǎn)與抗體之間相互作用的強(qiáng)度表示為抗體對(duì)抗原的親和力。抗體“臂”的可變區(qū)通過(guò)每個(gè)抗原位點(diǎn)處的弱非共價(jià)力與抗原上的多個(gè)位點(diǎn)相互作用。互動(dòng)越多,親和力就越大。
親和力主要受三個(gè)因素控制:(1)抗體對(duì)表位的親和力,(2)抗原和抗體兩者的結(jié)合價(jià)(3)相互作用位點(diǎn)的構(gòu)型。最終,這些因素決定了抗體特異性,或者特定抗體與精確抗原表位結(jié)合的可能性。
交叉反應(yīng)性是指抗體或抗體群體與除觸發(fā)抗體產(chǎn)生的抗原之外的抗原上的表位的結(jié)合。這種情況的發(fā)生可能是由于抗體的親和力或特異性較低,或者是因?yàn)椴煌目乖哂邢嗤蚍浅O嗨频谋砦弧?
當(dāng)相關(guān)抗原基團(tuán)需要普遍結(jié)合時(shí),或者在表位的蛋白質(zhì)序列在進(jìn)化過(guò)程中不高度保守的情況下嘗試進(jìn)行種間標(biāo)記時(shí),可能需要交叉反應(yīng)性。
交叉反應(yīng)可能導(dǎo)致高估或低估抗原濃度,這是免疫測(cè)定中的一個(gè)問題。
免疫化學(xué)技術(shù)依賴于每種免疫球蛋白對(duì)其各自抗原的極端分子水平特異性,即使存在高水平的污染分子。大多數(shù)抗原和抗體具有多個(gè)相互作用位點(diǎn),相互作用后會(huì)形成沉淀。使用抗體的實(shí)驗(yàn)示例包括蛋白質(zhì)印跡、免疫組織化學(xué)和免疫細(xì)胞化學(xué)、酶聯(lián)免疫吸附測(cè)定 (ELISA)、免疫沉淀和流式細(xì)胞術(shù)。
抗原和抗體之間的特異性結(jié)合是由于氫鍵、疏水相互作用、靜電力和范德華力。盡管這些力中的每一個(gè)都是弱非共價(jià)鍵,但抗原和抗體之間的結(jié)合可以非常強(qiáng)。
與抗體一樣,抗原可以具有多個(gè)相互作用位點(diǎn),例如具有相同表位的多個(gè)拷貝或具有被多個(gè)抗體識(shí)別的多個(gè)表位。涉及多個(gè)相互作用位點(diǎn)的結(jié)合會(huì)導(dǎo)致形成更穩(wěn)定的復(fù)合物,但也會(huì)引入構(gòu)象干擾,從而降低結(jié)合的可能性。
所有抗原-抗體結(jié)合都是可逆的,并遵循適用于可逆雙分子相互作用的基本熱力學(xué)原理。
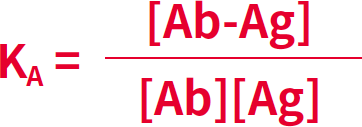
KA是親和常數(shù),[Ab-Ag] 是抗原抗體復(fù)合物的摩爾濃度,[Ab] 和 [Ag] 是抗體 (Ab) 或抗原 (Ag) 中游離的、非相互作用的結(jié)合位點(diǎn)分別代表摩爾濃度
達(dá)到平衡所需的時(shí)間取決于擴(kuò)散速率和抗體對(duì)抗原的親和力,并且可能有很大差異。抗體-抗原結(jié)合的親和常數(shù)也可以在很寬的范圍內(nèi)變化,范圍從小于10 5 /mol到大于10 12 /mol。親和常數(shù)受溫度、pH 值和溶劑的影響。雖然可以測(cè)定單克隆抗體的親和常數(shù),但不可能測(cè)定多克隆抗體的親和常數(shù),因?yàn)槎嗫寺】贵w和抗原之間形成多重鍵。
抗體對(duì)抗原的親和力的定量測(cè)量可以通過(guò)平衡透析進(jìn)行。通過(guò)保持抗體濃度恒定并在改變配體濃度的同時(shí)重復(fù)平衡透析來(lái)創(chuàng)建斯卡查德圖。該圖提供了有關(guān)親和力和潛在交叉反應(yīng)性的信息。
在設(shè)計(jì)實(shí)驗(yàn)程序時(shí)區(qū)分單克隆抗體和多克隆抗體非常重要,因?yàn)閱慰寺】贵w和多克隆抗體之間的差異在其使用中各有優(yōu)缺點(diǎn)。
抗體的結(jié)合位點(diǎn)位于抗體分子的F(ab)部分,該部分由重鏈和輕鏈的高變區(qū)組成。該位點(diǎn)與抗原結(jié)合的特點(diǎn)及過(guò)程如下。
抗原抗體反應(yīng)可能受到多種因素的影響。常見因素包括:
溫度
抗原-抗體反應(yīng)的最佳溫度取決于表位或互補(bǔ)位的化學(xué)性質(zhì)以及參與這些相互作用的鍵的類型。例如,氫鍵的形成往往是放熱的。使用碳水化合物抗原時(shí),溫度很重要,因?yàn)檫@些鍵在較低溫度下更穩(wěn)定。
pH值
pH 對(duì)抗原抗體復(fù)合物平衡常數(shù)的影響發(fā)生在 pH 6.5 至 8.4 之間。當(dāng)pH低于6.5和高于8.4時(shí),抗原抗體反應(yīng)受到強(qiáng)烈抑制。pH 5.0 或 9.5 時(shí)的平衡常數(shù)比 pH 6.5-7.0 時(shí)小 100 倍。在極端 pH 條件下,抗體可能會(huì)發(fā)生構(gòu)象變化,從而損害其與抗原的互補(bǔ)性。
離子強(qiáng)度
離子強(qiáng)度對(duì)抗原抗體反應(yīng)的影響在血型血清學(xué)中尤為重要,其中鈉離子和氯離子對(duì)反應(yīng)有顯著影響。例如,在生理鹽水中,Na +和 Cl -聚集在復(fù)合物周圍,部分中和電荷,從而可能干擾抗體與抗原的結(jié)合。當(dāng)使用低親和力抗體時(shí),這可能是一個(gè)問題。眾所周知,γ-球蛋白會(huì)凝集,與紅細(xì)胞脂蛋白形成可逆復(fù)合物,并在暴露于極低離子強(qiáng)度時(shí)沉淀。
上面,我們解釋了抗原抗體復(fù)合物形成中涉及的“抗原抗體相互作用”。抗原抗體復(fù)合物的形成是免疫化學(xué)的基本原理。理解好原理,用好抗體技術(shù)。